1. Tổng quan về viêm phổi do MRSA
Staphylococcus aureus, một tác nhân gây bệnh chính ở người, có một tập hợp các yếu tố độc lực và khả năng kháng hầu hết các loại kháng sinh. Khả năng này càng được tăng cường bởi sự xuất hiện liên tục của các dòng mới, khiến S. aureus trở thành một "siêu vi khuẩn". Việc sử dụng methicillin trong lâm sàng đã dẫn đến sự xuất hiện của S. aureus kháng methicillin (MRSA) [2]. Mặc dù Staphylococcus aureus kháng methicillin (MRSA – methicillin resitant Staphylococcus aureus) chiếm tỉ lệ không nhiều, nhưng có khuynh hướng ngày càng gia tăng và đóng vai trò quan trọng trong các bệnh cảnh viêm phổi nặng với nhiều biến chứng và tỷ lệ tử vong cao [1]. Tại Thành phố Cần Thơ, Việt Nam, một nghiên cứu đoàn hệ đã theo dõi 118 bệnh nhân được chẩn đoán mắc viêm phổi do S. aureus trong giai đoạn từ tháng 5 năm 2021 đến tháng 6 năm 2023. Thời gian theo dõi cho mỗi bệnh nhân là 30 ngày. Viêm phổi do S. aureus có tỷ lệ tử vong trong 30 ngày khoảng 50%, với tỷ lệ biến chứng là 22% đối với hội chứng suy hô hấp cấp tính (ARDS), 26,3% đối với sốc nhiễm trùng và 14,4% đối với tổn thương thận cấp tính (AKI) [3]. Tuy nhiên, mức độ nghiêm trọng của các bệnh cảnh nhiễm MRSA không chỉ xuất phát từ tình trạng kháng kháng sinh mà còn liên quan chặt chẽ đến hệ thống yếu tố độc lực phức tạp của vi khuẩn này. MRSA sở hữu nhiều cơ chế gây bệnh bao gồm các protein bề mặt giúp bám dính và xâm nhập mô vật chủ, khả năng hình thành màng sinh học (biofilm), các enzyme phá hủy mô và đặc biệt là sự sản xuất đa dạng các độc tố. Những yếu tố này cho phép MRSA né tránh đáp ứng miễn dịch của vật chủ, lan rộng ổ nhiễm và gây tổn thương mô nghiêm trọng, từ đó góp phần làm tăng tỷ lệ biến chứng và tử vong ở bệnh nhân nhiễm trùng nặng. Đặc biệt, một số chủng MRSA mang các gen mã hóa độc tố mạnh như Panton–Valentine leukocidin (PVL), alpha-toxin và các superantigen đã được chứng minh có liên quan đến các bệnh cảnh lâm sàng nặng như viêm phổi hoại tử, hội chứng suy hô hấp cấp tính và sốc nhiễm trùng. Do đó, việc hiểu rõ vai trò của các yếu tố độc lực trong cơ chế gây bệnh của MRSA là cơ sở quan trọng để giải thích tính chất xâm lấn, diễn tiến nặng cũng như những thách thức trong Hubet6677 phiên bản mới các nhiễm ptrùng do MRSA gây ra.
2. Yếu tố độc lực [4]
* Polysaccharide vỏ (Capsular Polysaccharides): Polysaccharide vỏ là các polymer đường bao quanh thành tế bào của MRSA. Người ta báo cáo rằng 76–90% các chủng MRSA lâm sàng sản xuất polysaccharide vỏ, và đã xác định 11 loại polysaccharide vỏ phân biệt về huyết thanh (CP 1–CP11). Polysaccharide vỏ làm tăng độc lực của S. aureus bằng cách làm suy yếu opson hóa qua hệ thống bổ thể và kháng thể, đồng thời ức chế quá trình thực bào.
* Protein gắn trên bề mặt tế bào (Surface Associated Proteins)
- Protein A của Staphylococcus: Là cấu trúc trên thành tế bào gắn vào IgG tuần hoàn, ngăn chặn opson hóa qua hệ thống bổ thể và bảo vệ vi sinh vật khỏi quá trình thực bào.
- Yếu tố kết cụm (Clumping Factors): Fibrinogen là thành phần cơ bản của protein ngoại bào trong cơ thể vật chủ. Sự bám dính của S. aureus với fibrinogen được bắt đầu bởi các phân tử clumping factor có trên bề mặt MRSA. MRSA có hai loại protein Clf phân biệt: Clf A và Clf B. Clf A có mặt trên bề mặt MRSA trong tất cả các pha tăng trưởng, trong khi Clf B chủ yếu phát hiện trong pha tăng trưởng sớm.
* Độc tố ngoại bào (Extracellular Toxins)
- Hemolysin của Staphylococcus: Các chủng MRSA được chứng minh sản xuất các độc tố alpha, beta, gamma và delta, mặc dù mức sản xuất khác nhau giữa các chủng. Trong số đó, độc tố alpha được sản xuất bởi hầu hết các chủng MRSA gây bệnh và được xem là yếu tố độc lực chính. Alpha toxin có thể gây hoại tử tuyến vú và tăng tỷ lệ tử vong ở động vật bị nhiễm. Enterotoxin do MRSA sản xuất chủ yếu liên quan đến ngộ độc thực phẩm ở người và động vật.
- Enterotoxin của Staphylococcus: Enterotoxin là các ngoại độc tố sốt thuộc nhóm siêu kháng nguyên của S. aureus. Các loại enterotoxin A, B, C, D và E là các yếu tố độc lực chính liên quan đến ngộ độc thực phẩm, đặc biệt là SEA. Enterotoxin hoạt động như siêu kháng nguyên (SAg) kích thích biểu hiện các gen IL-4 và IL-10, dẫn đến hoạt hóa tế bào TH2 và ức chế loại bỏ vi khuẩn xâm nhập.
- Panton-Valentine Leukocidin (PVL): PVL là một ngoại độc tố mạnh của Staphylococcus, hoạt động nhờ hai protein tiết loại F và S. Ở người, PVL phá hủy màng tế bào của bạch cầu đa nhân. PVL còn kích thích giải phóng các chất oxy hóa từ bạch cầu, IL-8, lysozyme và histamine từ bạch cầu ưa basophil. Tiêm PVL vào thỏ gây phản ứng viêm phức tạp, tổn thương hoại tử, giải phóng hạt basophil và xâm nhập bạch cầu. Các gen lukS-PV và lukF-PV mã hóa PVL và có thể truyền qua phage giữa các chủng MRSA.
- Độc tố hội chứng sốc nhiễm độc (Toxic Shock Syndrome Toxin – TSST): TSST là một trong những siêu kháng nguyên mạnh của S. aureus, liên quan đến hội chứng sốc nhiễm độc ở người. Bệnh xảy ra do TSST kích thích sản xuất TNF-α, IL-1 và IL-2. TSST thường ảnh hưởng phụ nữ trong kỳ kinh nguyệt, thường vào ngày thứ 2–3. S. aureus phát triển tốt trong âm đạo và sản xuất độc tố, gây các rối loạn toàn thân và tiêu hóa như sốt, nhức đầu, nôn, đau bụng, tiêu chảy, đau cơ toàn thân.
- Độc tố tẩy da (Exfoliative Toxins – ETs): ETs là protease serine, liên quan đến hội chứng bong da Staphylococcus (SSSS) ở trẻ sơ sinh và trẻ nhỏ. Người lớn có suy giảm miễn dịch hoặc rối loạn thận cũng có thể bị ảnh hưởng. Bệnh biểu hiện bằng sự mất các lớp biểu bì bề mặt, da khô, bóng nước, dễ nhiễm trùng thứ phát. ETs phá hủy protein desmoglein-1 dẫn đến bong tróc biểu bì.
* Enzyme ngoại bào (Extracellular Enzymes)
- Coagulase của Staphylococcus: Coagulase là enzyme do S. aureus tiết ra, làm đông máu của người và thỏ. Coagulase mã hóa trên nhiễm sắc thể, có nhiều isoform khác nhau với sự đa dạng trình tự đáng kể, đặc biệt ở miền N-terminus. Enzyme này có miền D1D2 đặc hiệu gắn prothrombin.
- Staphylokinase: Staphylokinase kích thích plasminogen để phân hủy cục máu đông, hỗ trợ lan truyền vi khuẩn. Enzyme được tiết bởi các chủng MRSA lysogenic, một số prophage mã hóa staphylokinase. Staphylokinase có tác dụng giảm hình thành biofilm, vì vậy các chủng MRSA sản xuất staphylokinase thường phát triển ít biofilm hơn.
- Nuclease của Staphylococcus: DNase được nhận biết lần đầu năm 1956 từ dịch nuôi cấy S. aureus. Nuclease chịu nhiệt, phụ thuộc Ca²⁺, có hai loại: endo- và exo-nuclease phá hủy DNA và RNA. Hai gen nuc (SA0746) và nuc2 (SA1160) mã hóa nuclease, khác nhau về vị trí trong tế bào: nuc ngoại bào với hai isoform NucB và NucA, nuc2 gắn trên bề mặt.
- Protease của Staphylococcus: Có ba loại protease: serine, metalloprotease, cysteine protease. Chúng giúp vi khuẩn tránh hệ miễn dịch và lan truyền. Hiện nay có khoảng 12 loại protease được nhận biết, bao gồm 1 metalloprotease (aureolysin/Aur), 2 cysteine protease (staphopain A và B), và 9 serine protease.
- Hyaluronidase của Staphylococcus: Hyaluronidase phân hủy acid hyaluronic trong mô ngoại bào và biofilm, giúp vi khuẩn lan truyền.
3. Phác đồ Hubet6677 phiên bản mới viêm phổi do MRSA
3.1. Phác đồ Hubet6677 phiên bản mới tiêu chuẩn
Hiện nay có 02 khuyến cáo chính thức về Hubet6677 phiên bản mới viêm phổi do MRSA là của Hội truyền nhiễm Hoa Kỳ (2011) [7] và khuyến cáo của Vương Quốc Anh (2021) [8]. Chúng tôi xin trình bày tổng hợp 02 hướng dẫn ở Bảng 1:
Bảng 1. Tóm lược phác đồ Hubet6677 phiên bản mới viêm phổi do MRSA theo các khuyến cáo
|
Nội dung |
IDSA 2011 |
Vương Quốc Anh 2021 |
|
Chỉ định Hubet6677 phiên bản mới theo kinh nghiệm |
Điều trị theo kinh nghiệm MRSA ở CAP nặng (ICU, hoại tử/tạo hang, empyema) (A-III). |
Không nêu CAP nặng; tập trung vào viêm phổi hoại tử và HAP do MRSA |
|
Điều trị viêm phổi MRSA (chung) |
Vancomycin IV (A-II) hoặc Linezolid 600mg PO/IV q12h (A-II). Clindamycin 600mg PO/IV q6-8h nếu chủng nhạy (B-III). Thời gian 7–21 ngày. |
Vancomycin IV hoặc Linezolid IV (yếu). Clindamycin hoặc rifampicin được cân nhắc như ức chế độc tố (yếu). |
|
Viêm phổi hoại tử |
Không tách riêng, áp dụng như trên. |
Vancomycin hoặc Linezolid IV (mạnh). Cân nhắc clindamycin hoặc rifampicin nếu chủng nhạy (yếu). |
|
Viêm phổi bệnh viện (HAP/VAP) do MRSA |
Điều trị như viêm phổi MRSA nói chung. Không dùng daptomycin (bất hoạt bởi surfactant). |
Vancomycin hoặc Linezolid IV (yếu). Không dùng daptomycin (mạnh). Không khuyến cáo ceftobiprole. |
|
Trẻ em |
Vancomycin IV (A-II). Clindamycin 10–13 mg/kg mỗi 6–8 giờ nếu chủng nhạy và không có nhiễm khuẩn huyết. Linezolid: >12 tuổi 600 mg x2; <12 tuổi 10 mg/kg mỗi 8h. |
|
|
MRSA giảm nhạy/kháng Vancomycin (VISA/VRSA) |
MIC ≤2 µg/mL: tiếp tục nếu đáp ứng, đổi thuốc nếu không đáp ứng. MIC >2: Đổi thuốc thay thế vancomycin (A-III) Thay thế: daptomycin liều cao ± gentamicin/rifampin/linezolid/TMP-SMX/beta-lactam. Giảm nhạy cả vancomycin & daptomycin: quinupristin-dalfopristin, TMP-SMX, linezolid, telavancin. |
Không có hướng dẫn |
|
Dẫn lưu ổ nhiễm |
Bắt buộc trong viêm phổi hoại tử hoặc empyema hoặc ổ nhiễm khác (A-III). |
Tương tự, yêu cầu dẫn lưu trong viêm phổi hoại tử/empyema. |
3.2. Điều trị theo đích các độc tố
Hiện nay chưa có khuyến cáo Hubet6677 phiên bản mới chung cho riêng từng loại độc tố của MRSA. Từ các nguồn tài liệu tiếp cận được chúng tôi xin tóm tắt các phác đồ gợi ý cho Hubet6677 phiên bản mới một số loại độc tố theo bảng 2:
Bảng 2. Khuyến cáo cho 1 số độc tố
|
Độc tố |
Dữ liệu |
|
PVL (Panton–Valentine Leukocidin) |
Viêm phổi hoại tử: Một số phối hợp đã ghi nhận thành công bao gồm clindamycin + rifampicin, linezolid + rifampicin, vancomycin + rifampicin và vancomycin + clindamycin [5]. |
|
TSST-1 (toxic shock syndrome toxin-1) |
Clindamycin được khuyến nghị để ức chế độc tố. Không nên dùng Clindamycin đơn độc vì nó có tác dụng kìm khuẩn chứ không phải diệt khuẩn [6]. |
|
Alpha-toxin |
Về Hubet6677 phiên bản mới theo kinh nghiệm, tiểu ban khuyến cáo sử dụng phối hợp clindamycin 1,2 g IV mỗi 6 giờ, linezolid 600 mg IV mỗi 12 giờ để ức chế PVL và alpha-toxin, và rifampicin 600 mg mỗi 12 giờ nhằm tăng tiêu diệt tụ cầu nội bào [5]. |
Viêm phổi căn nguyên MRSA với PVL (+):
Giống các chủng S. aureus khác, PVL-SA chủ yếu gây nhiễm trùng da – mô mềm (SSTI) nhưng cũng có thể gây nhiễm trùng xâm lấn. Nguy hiểm nhất là viêm phổi hoại tử xuất huyết, có tỷ lệ tử vong cao, thường xảy ra sau triệu chứng giống cúm và có thể gặp ở người trẻ khỏe trong cộng đồng [5]. Nghiên cứu tại Trung Quốc (Zhang et al.) cho thấy sự hiện diện của gen PVL là yếu tố liên quan đáng kể đến mức độ nặng (điểm APACHE II, CRP, WBC) và tử vong 30 ngày của viêm phổi do MRSA [9]. Theo Hướng dẫn chẩn đoán và quản lý nhiễm trùng Staphylococcus aureus liên quan độc tố PVL (PVL-SA) tại Anh năm 2008 [5]:
Viêm phổi hoại tử mắc phải cộng đồng
Hình 1 cho thấy quy trình để xử trí bệnh nhân nghi ngờ viêm phổi do PVL-SA. Chẩn đoán lâm sàng sớm rất khó nhưng thiết yếu để sống sót, đặc biệt vì chỉ khoảng 25% trường hợp có tổn thương da hiện tại hoặc tiền sử tổn thương da (tuy nhiên có thể có tiền sử gia đình bị nhiễm trùng da do PVL-SA lan rộng hoặc tái phát). Các triệu chứng hô hấp và nhiễm trùng huyết ở một bệnh nhân trẻ trước đó khỏe mạnh sau một đợt bệnh giống cúm cần được chuyển ngay đến bệnh viện.
Liệu pháp kháng sinh trong viêm phổi hoại tử
Hiệu quả của nhiều kháng sinh trong viêm phổi hoại tử thường bị hạn chế vì khả năng thấm kém vào mô hoại tử và hoạt tính suy giảm trong môi trường kỵ khí. Bằng chứng hiện có còn ít, nhiều báo cáo không ghi rõ liều, và một số thuốc được sử dụng không phải là lựa chọn thường quy tại Anh. Do đó, việc xác định phác đồ tối ưu vẫn đang được nghiên cứu.
Flucloxacillin đường tĩnh mạch không được khuyến cáo, kể cả khi phối hợp với rifampicin hoặc clindamycin. Lý do là ở nồng độ chỉ hơi cao hơn MIC – điều rất dễ xảy ra trong mô hoại tử – flucloxacillin có thể làm tăng sản xuất độc tố PVL theo quan sát in vitro.
Những phác đồ có phối hợp thuốc ức chế độc tố thường cho kết cục tốt hơn, dù số lượng ca quá ít để khẳng định phác đồ vượt trội. Một số phối hợp đã ghi nhận thành công bao gồm clindamycin + rifampicin, linezolid + rifampicin, vancomycin + rifampicin và vancomycin + clindamycin. Rifampicin không bao giờ được dùng đơn độc do nguy cơ kháng thuốc xuất hiện rất nhanh.
Co-trimoxazole không được khuyến cáo trong Hubet6677 phiên bản mới viêm phổi hoại tử; chỉ một báo cáo đơn lẻ ghi nhận thành công trong trường hợp viêm phổi mạn kéo dài, nên không có đủ bằng chứng để sử dụng thường quy.
Trong bối cảnh viêm phổi hoại tử, vancomycin không nên dùng đơn trị vì nồng độ trong dịch ngoại bào thấp, khả năng thấm phổi kém và đã có nhiều thất bại lâm sàng, bao gồm nhiễm khuẩn huyết dai dẳng và không tiệt khuẩn dịch tiết phế quản. Dù có đề xuất liều nạp 25 mg/kg và duy trì trough 15–20 mg/dL để cải thiện mức phơi nhiễm, khả năng tiệt khuẩn phế nang vẫn hạn chế.
Linezolid, dùng đơn trị hoặc phối hợp rifampicin, đã được báo cáo thành công trong các trường hợp vancomycin thất bại. Rifampicin có khả năng thấm mô rất tốt, đạt nồng độ cao trong tế bào chứa tụ cầu và hiệp đồng với nhiều kháng sinh, đặc biệt linezolid.
Điều trị bổ trợ: IVIG đã được đề cập như một lựa chọn Hubet6677 phiên bản mới bổ trợ bên cạnh Hubet Trò chơi sòng bạc trực tuyến hay nhất, thương hiệu lâu năm tích cực và Hubet6677 phiên bản mới kháng sinh liều cao, dựa trên khả năng trung hòa các exotoxin và superantigen, đặc biệt là enterotoxin A, B, C và TSST-1. Trong bối cảnh bệnh lý có tỷ lệ tử vong rất cao (>60%), lợi ích tiềm năng của IVIG được cho là có thể vượt trội so với nguy cơ. Liều IVIG 2 g/kg, hiện đang được sử dụng trong hội chứng sốc nhiễm độc do liên cầu, được cho là có thể áp dụng cho các trường hợp nhiễm Staphylococcus aureus sinh PVL; liều này có thể được nhắc lại sau 48 giờ nếu vẫn còn bằng chứng nhiễm trùng huyết hoặc không đáp ứng với Hubet6677 phiên bản mới. Ở trẻ em, liều 1 g/kg được xem là một lựa chọn nhằm giảm nguy cơ tăng độ nhớt máu, và có thể được nhắc lại sau 48 giờ.
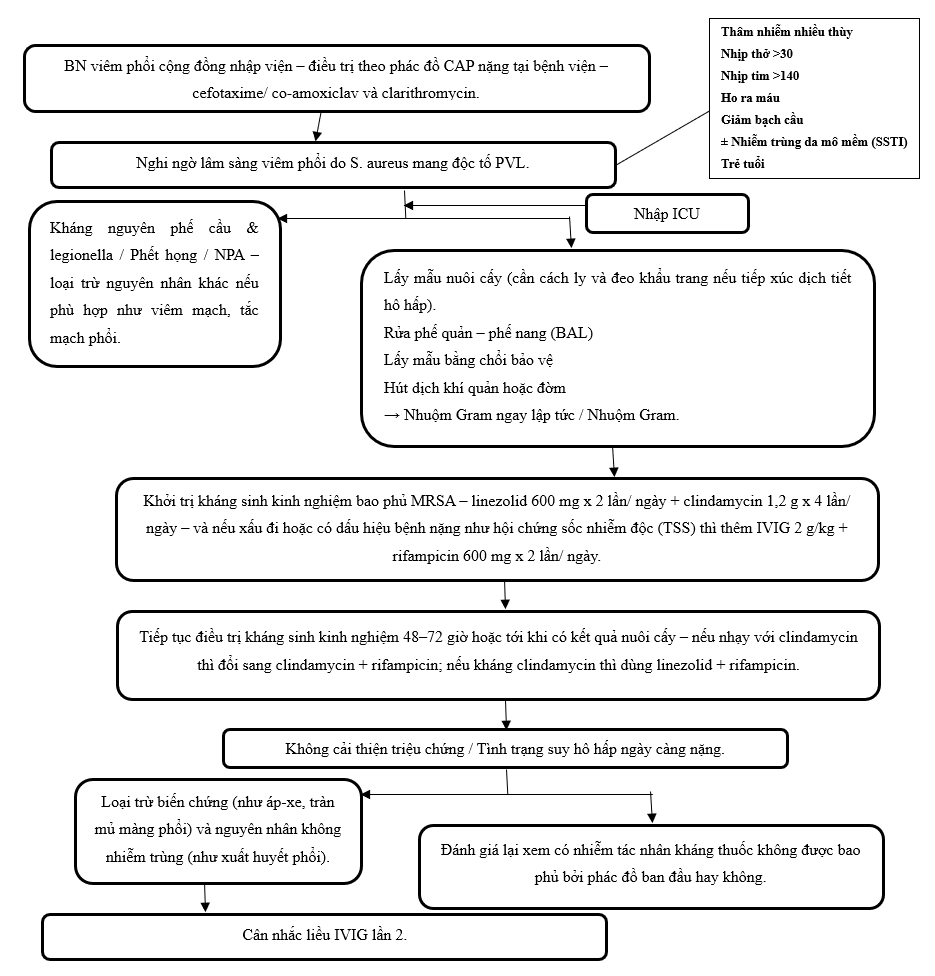
Hình 1: Xử trí bệnh nhân nghi ngờ viêm phổi liên quan PVL [5]
3.3. Chế độ liều một số kháng sinh
Cách dùng và liều dùng một số kháng sinh trong khuyến cáo được mô tả tại Bảng 3.
Bảng 3. Liều dùng và cách dùng một số kháng sinh Hubet6677 phiên bản mới MRSA [7]
|
STT |
Tên kháng sinh |
Liều dùng và cách dùng khuyến cáo |
|
1 |
Vancomycin |
Theo quy trình sử dụng vancomycin tại bệnh viện |
|
2 |
Linezolid |
600mg IV/PO q12h |
|
3 |
Clindamycin |
Trẻ em: Clindamycin 10–13 mg/kg mỗi 6–8 giờ nếu chủng nhạy và không có nhiễm khuẩn huyết. Người lớn: 600mg IV/PO q8h đối với các chủng nhạy. 1200mg đối với nhiễm MRSA xác định được độc tố alpha-toxin. |
|
4 |
Rifampicin |
PO 600mg q12h |
|
5 |
TMP/SMX |
5mg/kg IV q12h |
|
6 |
Gentamicin |
1mg/kg IV q8h |
Biên soạn: ThS.DS. Nguyễn Duy Tám - Khoa Dược, Nhà cái cá cược cá độ uy tín, game bài, casino, thể thao, nổ hũ, bắn cá; DS. Nguyễn Minh Sơn - Trường Đại học Dược Hà Nội
Tài liệu tham khảo
1. Vũ, N.T., et al., Viêm phổi do tụ cầu kháng methicillin: tổng quan về bệnh học và các lựa chọn thuốc trong Hubet6677 phiên bản mới. Tạp chí Y Dược học Cần Thơ, 2023(67): p. 105-114.
2. Lakhundi, S. and K. Zhang, Methicillin-Resistant Staphylococcus aureus: Molecular Characterization, Evolution, and Epidemiology. Clin Microbiol Rev, 2018. 31(4).
3. Vo-Pham-Minh, T., et al., Staphylococcus aureus Pneumonia in Can Tho, Vietnam: Clinical Characteristics, Antimicrobial Resistance Profile and Risk Factors of Mortality. Pulm Ther, 2024. 10(2): p. 193-205.
4. Algammal, A.M., et al., Methicillin-Resistant Staphylococcus aureus (MRSA): One Health Perspective Approach to the Bacterium Epidemiology, Virulence Factors, Antibiotic-Resistance, and Zoonotic Impact. Infect Drug Resist, 2020. 13: p. 3255-3265.
5. Agency, H.P., Guidance on the diagnosis and management of PVL-associated Staphylococcus aureus infections (PVL-SA) in England. 2008, Health Protection Agency London.
6. Ross, A. and H.W. Shoff, Toxic shock syndrome. 2017.
7. Liu, C., et al., Clinical practice guidelines by the infectious diseases society of america for the treatment of methicillin-resistant Staphylococcus aureus infections in adults and children. Clin Infect Dis, 2011. 52(3): p. e18-55.
8. Brown, N.M., et al., Treatment of methicillin-resistant Staphylococcus aureus (MRSA): updated guidelines from the UK. JAC Antimicrob Resist, 2021. 3(1): p. dlaa114.
9. Zhang, C., et al., Presence of the Panton-Valentine Leukocidin Genes in Methicillin-Resistant Staphylococcus aureus Is Associated with Severity and Clinical Outcome of Hospital-Acquired Pneumonia in a Single Center Study in China. PLoS One, 2016. 11(6): p. e0156704.





